W badaniu Cosmetosafe Consulting wypowiedzieli się technolodzy kosmetyczni, pracownicy działów R&D. Jego celem było określenie najważniejszych potrzeb i wyzwań tej grupy zawodowej.
Według 76 proc. respondentów biorących udział w badaniu dużego lub bardzo dużego zaangażowania wymaga śledzenie zmian regulacyjnych a według 79 proc. zaangażowania wymagają reformulacje produktów związane z tymi zmianami.
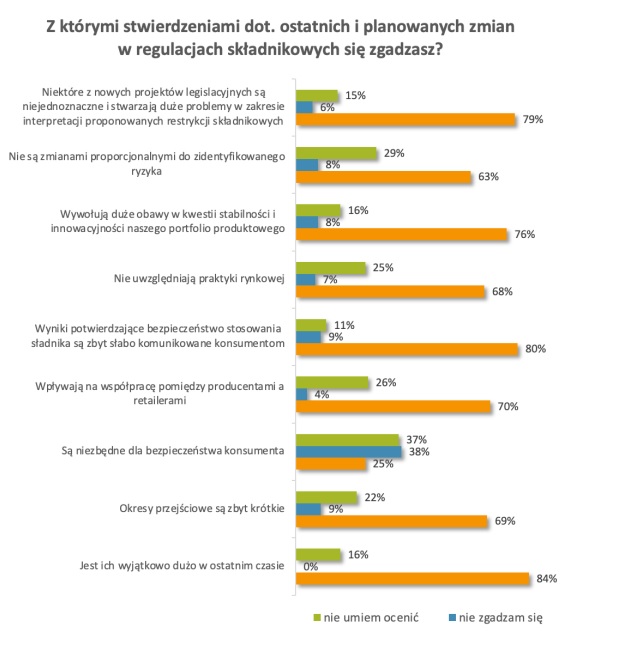
84 proc. technologów kosmetycznych uważa, że zmian w regulacjach składnikowych jest zbyt dużo. 79 proc. uważa, że niektóre z nowych regulacji są niejednoznaczne i stwarzają duże problemy w zakresie interpretacji proponowanych restrykcji składnikowych. 76 proc. obawia się, że zmiany te wpłyną na stabilność i innowacyjność portfolio produktowego firm.
Safety assessorzy z Cosmetosafe Consulting wskazują na następujące zmiany legislacyjne, które są nie do końca jednoznaczne lub zrozumiałe:
- Praktyczne rozwiązania w zakresie monitoringu zawartości oraz ewentualnych metod referencyjnych związanych ze zmianą preambuły do aneksu V w zakresie oznakowania „uwalnia formaldehyd” dla donorów formaldehydu (Rozp. (UE) nr 2022/1181).
- Interpretacja zapisów w zakresie ekspozycji na promieniowanie UV w odniesieniu do restrykcji dla Methyl-N-methylanthranilate (Rozp. (UE) nr 2022/135).
- Wprowadzony zakaz stosowania INCI: Methyl Salicylate w produktach dla dzieci < 6 roku życia (Rozp. (UE) nr 2022/1531)
- Ditlenek tytanu – oczekujemy konsekwencji unieważnienia Rozp. (UE) nr 2020/217 ws. klasyfikacji TiO2 jako substancji rakotwórczej przez Trybunał Sprawiedliwości Unii Europejskiej, decyzję TSUE opublikowano 23.11.2022
- Wszyscy pamiętamy zawirowania rynkowe związane z zakazem stosowania lilialu, w chwili obecnej oczekujemy publikacji rozporządzenia zakazującego stosowania teofiliny (planowana publikacja ok. połowy 2023 roku, a już wiemy, że zakaz będzie obowiązywał od grudnia b.r.!)
- Chyba jednak największe obawy wzbudza oczekiwana w niedalekiej przyszłości publikacja rozporządzenia w zakresie rozszerzenia wymagań indywidualnego oznakowania alergenów zapachowych – gdzie aktualna lista 24 substancji zostanie uzupełniona o kolejne ponad 50 pozycji!
70 proc. respondentów twierdzi, że regulacje składnikowe źle wpływają na współpracę na linii producenci kosmetyków-handel. 69 proc. wskazuje że okresy przejściowe dla produktów, w których zmiany składnikowe następują, są zbyt krótkie.
Aż 80 proc. uważa, że wyniki potwierdzające bezpieczeństwo składników kosmetycznych są zbyt słabo komunikowane konsumentom. Doprowadza to do sytuacji, w której nawet bezpieczny składnik jest wycofywany z rynku przez krążące w sieci mity konsumenckie i presję kupujących.
Autorzy raportu wskazują, że składników, które niesłusznie trafiają na tzw. czarne listy tworzone przez konsumentów jest bez liku i wskazują przykłady: dwutlenek tytanu, parabeny, związki glinu, chemiczne filtry UV, i wiele innych.
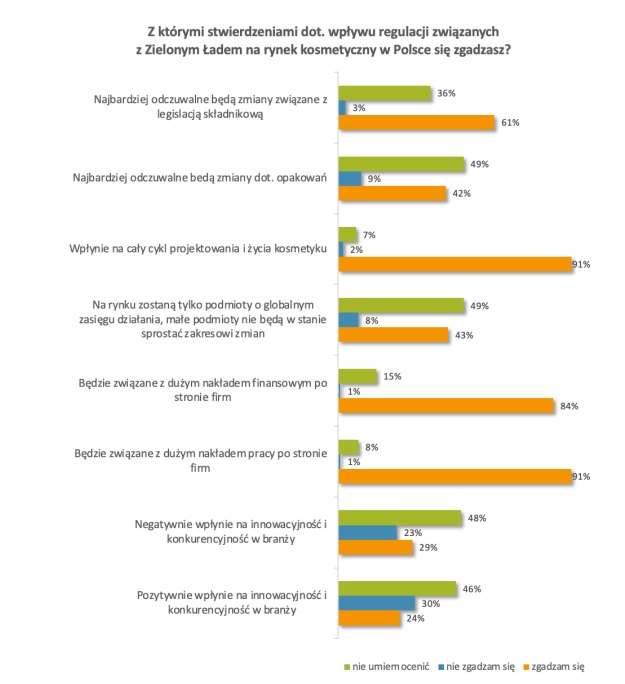
46 proc. respondentów biorących udział w badaniu Cosmetosafe Consulting nie umie przewidzieć, jaki będzie wpływ Zielonego Ładu na konkurencyjność branży kosmetycznej. 30 proc. ocenia go raczej negatywnie, a tylko niespełna ¼ badanych widzi pozytywy we wprowadzeniu nowych regulacji.
Według respondentów istnieje duże ryzyko, że na rynku zostaną tylko podmioty o globalnym zasięgu działania, gdyż małe podmioty nie będą w stanie sprostać zakresowi i tempu proponowanych zmian. Z tym stwierdzeniem zgadza się 43 proc. badanych, a 49 proc. nie umie dziś tego ocenić.
To, co widać na pewno to fakt, że wprowadzenie zasad Green Deal wpłynie na cały cykl projektowania i życia kosmetyku (91 proc.). Będzie związane z dużym nakładem pracy po stronie firm (tak uważa 91 proc. badanych) oraz dużym nakładem finansowym (84 proc.).
61 proc. badanych potwierdza, że w ich odczuciu najbardziej zauważalne będą zmiany związane z legislacją składnikową, a 49 proc. uważa ponadto, że będą to zmiany w zakresie opakowań.
Druga tura badania Cosmetosafe Consulting została przeprowadzona w dn. 24.01-27.03.2023 metodą wywiadów online (CAWI) na panelu internetowym Webankieta. Przeprowadzono 99 ankiet z pracownikami działów badawczo-rozwojowych (R&D) z branży kosmetycznej w firmach o różnym stopniu rozwoju i wielkości. Ponad 50 proc. ankietowanych stanowiły osoby pracujące na stanowiskach: dyrektor, kierownik, manager działu R&D, starszy specjalista, ekspert R&D.
Cosmetosafe Consulting to założona w 2013 przez dr inż. Iwonę Białas firma doradcza specjalizująca się w udzielaniu wsparcia regulacyjnego, naukowego i technicznego firmom z branży kosmetycznej (ocena bezpieczeństwa, uzasadnianie deklaracji marketingowych, wsparcie regulacyjne przy wprowadzaniu i opracowywaniu koncepcji produktowych czy w zakresie zgodności z przepisami oraz przy kontrolach organów).
Czytaj także:
Surowce kosmetyczne poszukiwane „na już” – technolodzy pod ogromną presją
Sieci handlowe tworzą własne listy zakazanych składników kosmetyków