
Sąd UE zadecydował, że trójwymiarowe opakowanie szminki Guerlain może być zarejestrowane jako znak towarowy. Sąd uchylił tym samym decyzję Pierwszej Izby Odwoławczej EUIPO (Urząd UE ds. Własności Intelektualnej), która uznała, że odmowa rejestracji tego znaku przez EUIPO była słuszna (Sprawa T-488/20). Chodzi o słynną szminkę Guerlain z lusterkiem, o rejestrację znaku towarowego firma wystąpiła 18 października 2018 r.
Znak towarowy, o którego zgłoszenie wystąpiła firma Guerlain
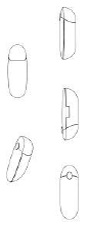
EUIPO uznało pierwotnie, że zgłoszone przez firmę trójwymiarowe opakowanie nie odbiega znacząco od zwykłych szminek dostępnych na rynku, o cylindrycznym kształcie. Stwierdzono także, że konsumenci są przyzwyczajeni do pojemników o owalnym kształcie. Zgłoszone oznaczenie nie posiadało według oceniających zdolności odróżniającej i nie zostało zarejestrowane jako znak towarowy. Pierwsza Izba Odwoławcza EUIPO oddaliła odwołanie firmy Guerlain, podtrzymując w mocy decyzję eksperta EUPIO stwierdzającą brak charakteru odróżniającego zgłoszonego znaku towarowego. Po zdefiniowaniu właściwego kręgu odbiorców i opisaniu tego znaku, uznała, że zwykłe szminki istniejące na rynku nie różnią się znacząco. Według niej wszystkie miały kształt cylindryczny, a konsumenci byli przyzwyczajeni do pojemników o owalnym kształcie.
Argumenty Guerlain
Firma Guerlin odwołała się od decyzji EUIPO utrzymując, że komisja błędnie zakończyła badanie charakteru odróżniającego zgłoszonego znaku towarowego, uznając, że nie odbiegał on w wystarczającym stopniu od normy lub zwyczajów branży. Wskazała na szereg uchybień. Podkreśliła, że zgłoszony znak towarowy składa się z nietypowego ogólnego kształtu kadłuba łodzi, kołyski lub odwróconej sztabki o zaokrąglonych krawędziach, z kopulastą górną częścią, która ma szczególnie odróżniający charakter. Udowadniała, że opakowanie szminki nie ma żadnej płaskiej powierzchni i nie może stać w pozycji pionowej. Nie mogła być ona zatem ona wystawiana, umieszczana ani przechowywana jak wszystkie inne produkty stanowiące standardowe lub zwykłe modele. To pokazuje, że forma produktu jest wyjątkowa i decyduje o jego postrzeganiu przez konsumentów. Dodatkowo opakowanie ma prostokątne wycięcie, które stanowi jego kolejną unikalną i jest postrzegane jako zawias, wskazujący na istnienie obrotowej pokrywy, która po otwarciu daje dostęp do lusterka.
Ponadto Guerlain podkreśliło, że oryginalny kształt opakowania szminki jest postrzegany przez konsumentów jako wyjątkowy, co potwierdza rynkowy sukces produktu. Świadczy o tym reakcja prasy i opinii publicznej, która jednogłośnie okrzyknęła formę szminki „rewolucyjną”
Decyzja sądu
W uzasadnieniu swojej decyzji Sąd UE zajął odmienne stanowisko od EUIPO. Jego zdaniem zgłoszony znak posiada charakter odróżniający właśnie dlatego, iż odbiega wyraźnie od norm i zwyczajów na rynku szminek – wyjaśnia kancelaria GKR Legal na swoim blogu.
Sąd przypomniał, że zgodnie z orzecznictwem ocena charakteru odróżniającego unijnego znaku towarowego nie opiera się na oryginalności lub braku używania tego znaku w dziedzinie danych towarów i usług. Także sama nowość kształtu trójwymiarowego znaku towarowego nie wystarcza do stwierdzenia istnienia takiego charakteru, ponieważ decydującym kryterium jest zdolność tego kształtu do pełnienia funkcji wskazania pochodzenia handlowego.
Potwierdzono, że nie można wykluczyć, że estetyczny wygląd znaku towarowego w postaci opakowania towaru, w tym przypadku jego pojemnika, może być brany pod uwagę, obok innych elementów, w celu stwierdzenia odmienności od normy i zwyczajów danej branży. Pod warunkiem jednak, że ów estetyczny wygląd jest rozumiany jako odnoszący się do obiektywnego i niezwykłego efektu wizualnego wywołanego przez określony wzór tego znaku towarowego.
Norma i zwyczaje sektora nie mogą być ograniczone do jedynego kształtu, który jest statystycznie najbardziej rozpowszechniony, lecz obejmują wszystkie kształty, które konsument jest przyzwyczajony widzieć na rynku. Biorąc zatem pod uwagę wzory uwzględnione przez Izbę Odwoławczą, jako stanowiące normę i zwyczaje w danym sektorze, należy stwierdzić, że przedmiotowy kształt jest nietypowy dla szminki i różni się od wszystkich innych kształtów istniejących na rynku. – Decyzja Sądu to dobry prognostyk dla producentów perfum i kosmetyków, stwarzająca możliwość rejestracji na ich rzecz odróżniających opakowań 3D – skomentowała mecenas Anna Gołębiowska.









